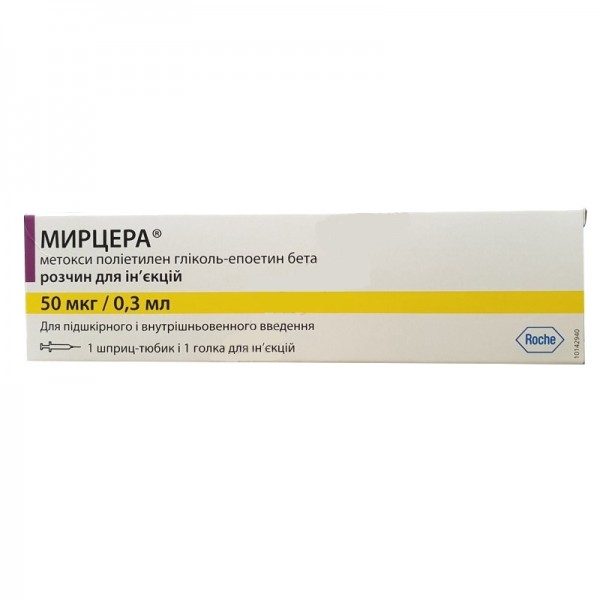
Мірцера 50 мкг 0.3 мл №1 шприц-тюбик
| Транспортна компанія | ||
- Оплата
- Гарантія
- Умови повернення
Готівкою при отриманні, оплата картою на сайті, накладений платіж
Опишіть симптоми або потрібний препарат — ми допоможемо підібрати його дозування чи аналог, оформимо замовлення з доставкою додому або просто проконсультуємо. Ми — це 28 фармацевтів і 0 ботів.
Так ми завжди будемо з вами на зв'язку і зможемо поспілкуватися в будь-який момент.
Опишіть симптоми або потрібний препарат — ми допоможемо підібрати його дозування чи аналог, оформимо замовлення з доставкою додому або просто проконсультуємо. Ми — це 28 фармацевтів і 0 ботів.
Так ми завжди будемо з вами на зв'язку і зможемо поспілкуватися в будь-який момент.
Властивості препарату Мірцера 50 мкг 0.3 мл №1 шприц-тюбик
Основні
| Діюча речовина | |
| Торгівельна назва | |
| Виробник | Рош Діагностикс ГмбХ, Німеччина для Ф. Хоффманн-Ля Рош ЛтД, Швейцарія, Німеччина/Швейцарія |
| Код АТС/ATX | B03X A03 |
| Код Моріон | 99880 |
| Лікарська форма | Розчин для ін'єкцій по 30 мкг/0,3 мл, 50 мкг/0,3 мл, 75 мкг/0,3 мл, 100 мкг/0,3 мл, 120 мкг/0,3 мл, 150 мкг/0,3 мл, 200 мкг/0,3 мл, 250 мкг/0,3 мл, 360 мкг/0,6 мл у шприц-тюбику № 1 |
| Міжнародна назва | Methoxy polyethylene glycol-epoetin beta |
| Кількість в упаковці | 1 |
| Дозування | 50 мкг |
| Об'єм | 0,3 мл |
| Форма випуску | Розчин для ін'єкцій |
| Фармакологічна група | Інші антианемічні засоби. |
Відгуки покупців 1
Опис Мірцера 50 мкг 0.3 мл №1 шприц-тюбик
При хронических болезнях почек наблюдается недостаточная выработка эритроцитов из-за нарушений синтеза веществ, которые отвечают за активацию этого процесса. Для нормализации процессов созревания эритроцитов используется Мирцера. Инструкция указывает, что препарат относится к антианемическим средствам.
Состав
Действующее вещество препарата – метокса. Приобрести вещество можно в виде раствора для инъекций, который помещен в шприц-тюбик. В 0.3 мл раствора содержится 50 мкг действующего компонента.
Показания
Основным показанием к применению препарата является:
-
нарушение формирования эритроцитов, и как следствие симптоматическая анемия, из-за хронического заболевания почек.
Перед тем, как представить препарат на рынке, проводилось длительное исследование его свойств и реакции, была доказана безопасность и эффективность Мирцера. Цена позволяет провести комплексное устранения анемии и нормализировать состояние вне зависимости от финансовых возможностей пациентов.
Противопоказания
В отзывах к препарату предоставляется информация о возможном возникновении индивидуальной непереносимости отдельных компонентов лекарственного средства, которая проявляется в аллергической реакции, анафилактическом шоке.
Применение и дозы
Применение препарата происходит только под присмотром врача с опытом проведения терапии больных с нарушениями в работе почек. Препарат вводится внутривенно и подкожно. Введение под кожу показано для пациентов, которые находятся на гемодиализе. Доза определяется в зависимости от уровня гемоглобина. При использовании препарата необходимо постоянно следить за уровнем гемоглобина 1 раз в 2 недели, чтобы избежать критического повышения. Начальная доза может составлять 0.6 мкг/кг и повышаться до 1.2 мкг/кг.
Чтобы узнать цену, точную характеристику представленного лекарственного средства, особенности его использования, побочные эффекты, необходимо изучить полную инструкцию к препарату.
Цена Мирцера 50 мкг 0.3 мл №1 шприц-тюбик актуальна при заказе на сайте. Купить Мирцера 50 мкг 0.3 мл №1 шприц-тюбик в городах Украины: Киев, Харьков, Днепр, Одесса, Ровно, Белая Церковь, Винница, Запорожье, Ивано-Франковск, Краматорск, Кременчуг, Кривой Рог, Кропивницкий, Львов, Луцк, Мариуполь, Николаев, Полтава, Сумы, Тернополь, Херсон, Житомир, Хмельницкий, Черкассы, Черновцы, Чернигов.
Ціна на Мірцера 50 мкг 0.3 мл №1 шприц-тюбик актуальна при замовленні на сайті. На apteka24.ua можна купити Мірцера 50 мкг 0.3 мл №1 шприц-тюбик з доставкою в такі міста України: Київ, Харків, Дніпро, Одеса, Рівне, Біла Церква, Вінниця, Запоріжжя, Івано-Франківськ, Краматорськ, Кременчук, Кривий Ріг, Кропивницький, Львів, Луцьк, Маріуполь, Миколаїв, Полтава, Суми, Тернопіль, Херсон, Житомир, Хмельницький, Черкаси, Чернівці, Чернігів. В інші міста замовлення можуть доставлятися через службу доставки. Доступна доставка кур'єром. Докладніше про способи, вартості та обмеженнях доставки.